Hội đồng Phản ứng có hại của thuốc (Medicines Adverse Reactions Committee - MARC) thuộc MEDSAFE đã công bố biên bản của cuộc họp Hội đồng định kỳ vào ngày 11/07/2017. Trong cuộc họp này, Hội đồng đã thảo luận về việc lắng đọng các thuốc cản quang có chứa gadolinium trong não
Thông tin chung
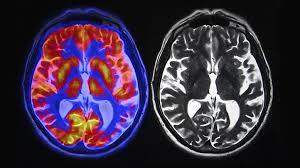
Các thuốc cản quan có chứa gadolinium (Gadolinium based contrast agents - GBCA) được tiêm cho bệnh nhân cần chụp MRI để giúp hiển thị hình ảnh các cơ quan nội tạng và mô tốt hơn. Sau khi vào cơ thể, các thuốc chứa gadolinium phần lớn được thải trừ qua thận nhưng có những nghiên cứu chỉ ra rằng có những lớp lắng đọng trong mô cơ thể, bao gồm não, da và xương.
Gần đây mối quan ngại về việc lắng đọng gadolinium trong não đã gia tăng. Trong khi EMA Việc lắng đọng này có gây độc hay không cần được làm sáng tỏ đầy đủ.
Động thái của một số cơ quan quản lý dược phẩm thế giới:
- Tháng 01/2017, Health Canada thông báo kết quả của một đánh giá tổng quan về độ an toàn của các thuốc cản quang có chứa gadolinium và nguy cơ thuốcbị tích lũy trong não sau khi sử dụng. Mặc dù chưa phát hiện được trường hợp nào dẫn đến hậu quả nghiêm trọng nhưng HealthCanada vẫn yêu cầu các nhà sản xuất thuốc cập nhật thông tin này trên nhãn thuốc đối quang từ chứa gadolinium. Các cán bộ y tế được khuyến cáo hạn chế sử dụng các thuốc này và chỉ dùng khi thực sự cần thiết; dùng liều thấp nhất có hiệu quả; đánh giá cẩn thận lợi ích/ nguy cơ của mỗi bệnh nhân trước khi sử dụng liều lặp lại.
- Tháng 03/2017, tại Châu Âu, PRAC đã khuyến nghị tạm dừng lưu hành (suspension of the marketing authorisations) 4 thuốc cản quang nhóm gadolinium vì có bằng chứng có một lượng nhỏ gadolinium lắng đọng trong não sau khi sử dụng thuốc. Các chế phẩm đường tiêm mà PRAC lo ngại là gadobenic acid, gadodiamide, gadopentetic acid và gadoversetamide, được tiêm cho bệnh nhân để tăng cường hình ảnh khi chụp cộng hưởng từ (MRI).
- Tháng 05/2017, FDA (Hoa Kỳ) công bố chưa xác định được biến cố có hại nào liên quan đến việc lắng đọng gadolinium trong não. Tất cả các thuốc cản quang có chứa gadolinium đều có thể liên quan đến việc lắng đọng gadolinium trong não hoặc trong các loại mô khác của cơ thể. Tuy nhiên cho đến thời điểm hiện tại, FDA chưa tìm thấy bằng chứng gây hại cho sức khỏe của tình trạng này, do vậy FDA chưa giới hạn sử dụng các thuốc cản quang có chứa gadolinium. FDA sẽ tiếp tục tiến hành đánh giá độ an toàn của gadolinium và sẽ công bố khi có kết quả cuối cùng.
Ảnh minh họa: Internet.
Thảo luận của MARC
Hội đồng đã thảo luận về các bằng chứng hiện có, về việc sử dụng GBCAs ở New Zealand và các loại GBCAs khác nhau (mạch thẳng và mạch vòng).
Hội đồng nhận thấy có bằng chứng cho thấy gadolinium đã được tìm thấy trong não sau khi sử dụng tất cả các loại GBCAs hiện có. Lắng động có thể xảy ra với các GBCAs ít bền vững hơn, có ít bằng chứng lặng đọng khi sử dụng các GBCAs mạch vòng. Tuy nhiên cần lưu ý rằng việc sử dụng MRI trên người không phải là phương pháp trực tiếp định lượng gadolinium, vì vậy không chắc chắn gadolinium mạch vòng bị lắng đọng sau khi sử dụng. Hội đồng nhất trí rằng bằng chứng hiện có không cho thấy bất cứ tổn thương nào liên quan đến việc gadolinium lắng đọng trong não.
Hội đồng cho rằng việc sử dụng các GBCAs trong MRI nên được thay đổi để giảm thiểu nguy cơ xơ hóa hệ thống nguồn gốc thận (nephrogenic systemic fibrosis).
Hội đồng cho rằng tuy chưa có bằng chứng gây tổn hại rõ ràng nhưng vẫn cần phải thận trọng khi sử gadolinium và phản ứng chính thức của CQQL đối với thông tin này cần được thảo luận thêm. Tuy nhiên Hội đồng khuyến cáo cập nhận tờ HDSD của các chế phẩm GBCAs về nguy cơ lắng đọng này. Mặt khác, Hội đồng cho rằng bằng chứng hiện không gợi ý cho việc gadolinium có thể tồn tại lâu dài trong não sau khi sử dụng GBCAs và thông tin này nên được chuyển tải tới CBYT và người bệnh.
Các khuyến cáo của MARC
Hội đồng khuyến cáo Medsafe yêu cầu các công ty sản xuất, kinh doanh dược phẩm cập nhật tờ HDSD về nguy cơ lắng đọng gadolinium.
Hội đồng khuyến cáo Medsafe chuyển tải các nội dung mà Hội đồng đã thảo luận về vấn đề này tới CBYT và người bệnh.
Nguồn: http://www.medsafe.
Người tổng hợp: DS. Nguyễn Phương Thúy