Qua quá trình thu thập dữ liệu và đánh giá độ an toàn của thuốc, tính đến ngày 22/05/2017, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) chưa xác định được biến cố có hại nào liên quan đến việc gadolinium bị lắng đọng trong não sau khi sử dụng các thuốc cản quang có gadolinium để chiếu chụp.
Qua quá trình thu thập dữ liệu và đánh giá độ an toàn của thuốc, tính đến ngày 22/05/2017, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) chưa xác định được biến cố có hại nào liên quan đến việc gadolinium bị lắng đọng trong não sau khi sử dụng các thuốc cản quang có gadolinium để chiếu chụp. Tất cả các thuốc cản quang có chứa gadonilium đều có thể liên quan đến việc lắng đọng gadolinium trong não hoặc trong các loại mô khác của cơ thể. Tuy nhiên cho đến thời điểm hiện tại, FDA chưa tìm thấy bằng chứng cho thấy lắng đọng gadolinium trong não có khả năng gây hại cho sức khỏe, vì vậy FDA chưa giới hạn sử dụng của các thuốc có chứa gadolinium ở thời điểm này. FDA sẽ tiếp tục tiến hành đánh giá độ an toàn của các thuốc cản quang có chứa gadolinium và sẽ công bố khi có kết quả cuối cùng.
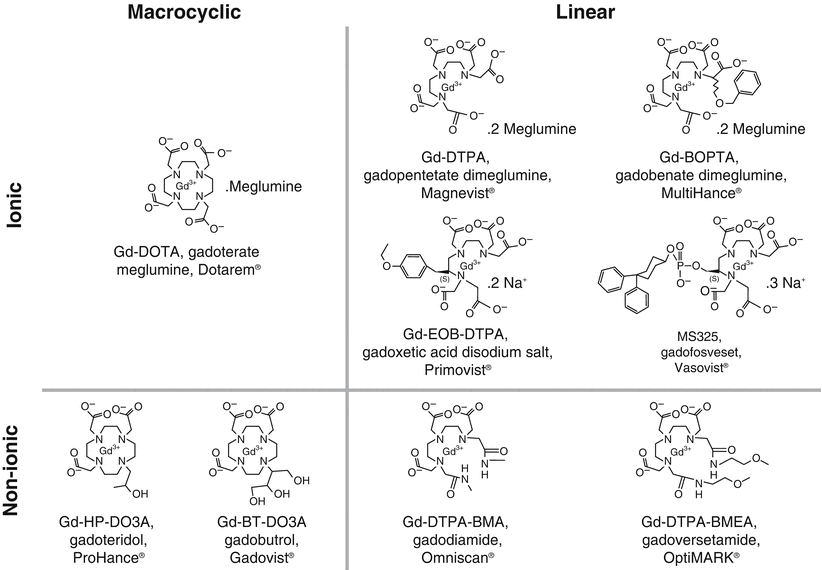
Gadolinium là một kim loại nặng có thể liên kết với các phân tử chất mang. Tiêm gadolinium vào ven giúp tăng chất lượng hình ảnh cộng hưởng, giúp cho cán bộ y tế có thể chẩn đoán tình trạng của các cơ quan trong cơ thể. Dựa trên cấu trúc hóa học, các thuốc cản quang có chứa gadolinium được phân làm hai loại: Thuốc cản quang chứa gadolinium mạch thẳng và Thuốc cản quang chứa gadolinium mạch vòng.
Ảnh minh họa: Internet.
FDA đã tiến hành phân tích các nghiên cứu và báo cáo phản ứng có hại liên quan đến các thuốc cản quang có chứa gadolinium. Một số nghiên cứu trên người và động vật cho thấy gadolinium có thể lắng đọng tại các cơ quan trong cơ thể như não, xương và da. Một số công bố chỉ ra rằng các thuốc cản quang chứa gadolinium mạch thẳng gây lắng đọng gadolinium trong não nhiều hơn so với thuốc cản quang chứa gadolinium mạch vòng. Tuy nhiên FDA không tìm thấy tác động có hại nào liên quan đến việc lắng đọng gadolinium trong não.
Cho đến thời điểm hiện tại, phản ứng có hại duy nhất đã biết liên quan đến việc lắng đọng gadolinium là tình trạng xơ hóa nguồn gốc thận (nephrogenic systemic fibrosis - NSF) xảy ra trên một nhóm nhỏ bệnh nhân có tiền sử suy thận. NSF làm xơ hóa da, gây đau đớn, ảnh hưởng tới các khớp xương và gây hạn chế vận động đáng kể trong vài tuần đến vài tháng. FDA cũng nhận được các báo cáo về những trường hợp xảy ra phản ứng xơ hóa ở da và các mô khác trên những bệnh nhân sử dụng GBCA có chức năng thận bình thường nhưng không phải là NSF, trong đó, một số bệnh nhân có bằng chứng lắng đọng gadolinium. FDA đang tiếp tục tiến hành phân tích những báo cáo như vậy để xác định liệu những phản ứng xơ hóa có phải là tác động có hại của việc lắng đọng gadolinium hay không.
Nhà sản xuất OptiMARK (gadoversetamide) – một GBCA có cấu trúc mạch thẳng đã cập nhật thông tin về lắng đọng gadolinium tại một số cơ quan như não, da… vào nhãn thuốc của mình. FDA cũng đang xem xét để quyết định có cần sửa đổi nhãn thuốc của các GBCA hay không.
Báo cáo gần đây của Ủy ban Đánh giá Nguy cơ Cảnh giác dược (PRAC) thuộc Cơ quan quản lý dược phẩm Châu Âu (European Medicines Agency - EMA) cũng xác định chưa tìm thấy tác động có hại nào liên quan đến việc lắng đọng gadolinium trong não nhưng PRAC khuyến cáo tạm dừng cấp số đăng ký của 4 GBCA mạch thẳng bởi chúng gây lắng đọng gadolinium trong não nhiều hơn các GBCA mạch vòng. Khuyến cáo của PRAC đang được EMA xem xét.
FDA vẫn đang tiếp tục đánh giá độ an toàn của các GBCA. Trung tâm nghiên cứu độc chất Quốc gia thuộc FDA đang tiến hành một nghiên cứu về lắng đọng GBCA trên não chuột và trên các cơ quan nội tạng khác. FDA sẽ liên tục cập nhật khi có thông tin mới và sẽ công bố khi có kết quả cuối cùng.
Nguồn: https://www.fda.gov/Drugs/DrugSafety/ucm559007.htm
Người tổng hợp: ThS. Nguyễn Phương Thúy