Tìm kiếm bài viết
-
HSA: Kiểu gen HLA-B*1502 và phản ứng trên da nghiêm trọng do carbamazepin
17/01/2017 12:00:00 SA:Việc sàng lọc kiểu gen HLA-B*1502 được thực hiện để phát hiện bệnh nhân có nguy cơ cao xảy ra SJS/TEN do carbamazepin. Tuy nhiên, việc sàng lọc kiểu gen không thể thay thế các biện pháp theo dõi bệnh ...
Xem tiếp >> -
HSA: Fluoroquinolon và nguy cơ bong võng mạc
17/01/2017 12:00:00 SA:Trong bản tin Adverse Drug Reaction News số 3 tập 18 - tháng 11/2016, HSA cảnh báo về nguy cơ bong võng mạc liên quan đến kháng sinh fluoroquinolon ...
Xem tiếp >> -
.jpg)
HSA: Giới hạn sử dụng các thuốc chứa codein trên trẻ em và trẻ vị thành niên
17/01/2017 12:00:00 SA:Trong bản tin Adverse Drug Reaction News số 3 tập 18 - tháng 11/2016, HSA khuyến cáo giới hạn sử dụng các thuốc chứa codein trên trẻ em và trẻ vị thành niên. ...
Xem tiếp >> -
Health Canada: Bản tin Health Product InfoWatch tháng 12/2016
17/01/2017 12:00:00 SA:Trong bản tin Health Product InfoWatch tháng 12/2016, Health Canada điểm một số thông tin an toàn thuốc liên quan đến các thuốc bisphosphonat, thuốc ức chế men DPP-4, loratadin, ondansetron, phenyleph ...
Xem tiếp >> -

US.FDA. Cập nhật lại về tác dụng bất lợi trên tâm thần của thuốc cai thuốc lá Chantix (vareniclin) và Zyban (bupropion)
16/01/2017 12:00:00 SA:Ngày 16/12/2016, dựa trên việc đánh giá một thử nghiệm lâm sàng lớn mà FDA yêu cầu các công ty dược tiến hành, FDA xác định nguy cơ tác dụng bất lợi nghiêm trọng trên tâm thần, hành vi, suy nghĩ khi ...
Xem tiếp >> -

TGA: cập nhật tổng quan về hiệu quả và độ an toàn của codein
16/01/2017 12:00:00 SA:Ngày 21/12/2016, TGA công bố tổng quan cập nhật về hiệu quả và độ an toàn của codein. Mục đích của tổng quan này nhằm xác định xem liệu có thêm bằng chứng nào về mối liên quan giữa hiệu quả và độ an t ...
Xem tiếp >> -
ANSM: nguy cơ phản ứng dị ứng chéo với thịt và nội tạng động vật liên quan đến dung dịch chứa gelatin biến tính đơn độc hay phối hợp
11/01/2017 12:00:00 SA:Khuyến cáo dành cho các cán bộ y tế (chuyên khoa cấp cứu, gây mê hồi sức và dược sỹ bệnh viện) về các chế phẩm có chứa dung dịch gelatin biến tính, không được sử dụng trên những bệnh nhân có: ...
Xem tiếp >> -
.jpg)
Vitamin D2 - Ergocalciferol (Biệt dược Uvestérol D) và trường hợp trẻ sơ sinh tử vong ở Pháp: Sai sót trong sử dụng thuốc?
11/01/2017 12:00:00 SA:Ngày 21/12/2016, một trẻ sơ sinh 10 ngày tuổi tại Pháp đã tử vong tại nhà do ngừng tim phổi. Hai tiếng sau khi bú sữa, trẻ được dùng một liều Uvestérol D và ngay lập tức có dấu hiệu ngạt thở và ngừng ...
Xem tiếp >> -
.jpg)
TGA: Nguy cơ huyết khối khi sử dụng thuốc tránh thai phối hợp dùng đường uống
11/01/2017 12:00:00 SA:Ngày 21/12/2016, Cơ quan Quản lý Điều trị Úc (TGA) thông báo đã hoàn thành tổng quan về nguy cơ huyết khối ở phụ nữ sử dụng thuốc tránh thai phối hợp dùng đường uống (CHC) chứa ethinyloestradiol và m ...
Xem tiếp >> -
TGA: Nguy cơ virus viêm gan B tái hoạt động
11/01/2017 12:00:00 SA:Ngày 19/12/2016, Cơ quan Quản lý Điều trị Úc (TGA) khuyến cáo cho người bệnh và cán bộ y tế về các thuốc điều trị virus viêm gan C tác dụng trực tiếp có liên quan tới sự tái khích hoạt virus viêm gan ...
Xem tiếp >> -
HealthCanada: Cập nhật thông tin về độ an toàn của các thuốc đối quang từ chứa gadolinium
11/01/2017 12:00:00 SA:Ngày 6/1/2017, HealthCanada thông báo vừa tiến hành một tổng quan về độ an toàn của các thuốc đối quang từ chứa gadolinium do nguy cơ các thuốc này có thể tích lũy trong não sau nhiều lần sử dụng. ...
Xem tiếp >> -
MHRA: Nguy cơ xuất hiện tác dụng bất lợi của corticosteroid đường toàn thân liên quan tới việc sử dụng đồng thời các thuốc tăng cường dược động học cho thuốc ARV (cobicistat, ritonavir) với các corticosteroid
07/01/2017 12:00:00 SA:Trong bản tin Drug Safety Update tháng 12/2016, MHRA cảnh báo về việc dùng đồng thời một corticosteroid với thuốc tăng cường dược động học cho thuốc ARV (cobicistat, ritonavir) có thể làm tăng nguy cơ ...
Xem tiếp >> -
MHRA: Phối hợp spironolacton và các thuốc tác động lên hệ renin-angiotensin theo đường toàn thân trong điều trị suy tim: Nêu rõ lại nguy cơ tăng kali máu nghiêm trọng có thể dẫn đến tử vong
28/12/2016 12:00:00 SA:Dựa trên thông tin phản hồi, Cơ quan Quản lý Dược phẩm Anh (Medicines and Healthcare products Regulatory Agency - MHRA) giải thích lại nội dung trong 1 bài báo đăng trên Drug Safety Update về việc sử ...
Xem tiếp >> -
US.FDA: Cảnh báo mới về việc sử dụng thuốc gây mê toàn thân và thuốc an thần cho trẻ nhỏ và phụ nữ có thai
17/12/2016 12:00:00 SA:Ngày 13/12/2016, Cơ quan Quản lý Thuốc và Thực phẩm Hoa Kỳ (US.FDA) thông báo về việc sử dụng thuốc gây mê toàn thân và thuốc an thần khi tiến hành phẫu thuật và thủ thuật ở trẻ nhỏ dưới 3 tuổi và phụ ...
Xem tiếp >> -
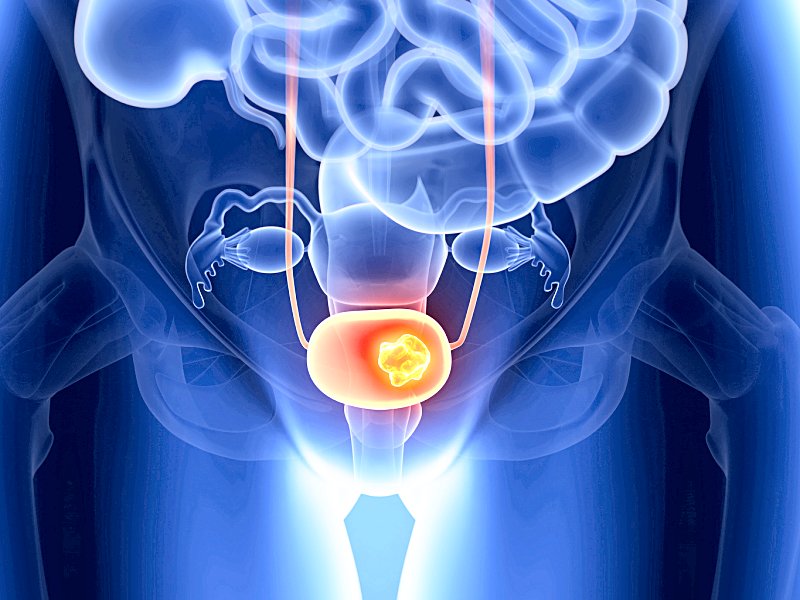
US.FDA: Cập nhật thông tin về tăng nguy cơ bàng quang liên quan đến pioglitazon
17/12/2016 12:00:00 SA:Ngày 12/12/2016, Cơ quan Quản lý Thuốc và Thực phẩm Hoa Kỳ (US.FDA) thông báo kết quả của cuộc rà soát mới đây về độ an toàn của các thuốc chứa pioglitazon. ...
Xem tiếp >>

.PNG)
.PNG)
.PNG)