LOOKUP MEDICINE INFOMATIONS
-

Bộ cơ sở dữ liệu thông tin thuốc bao gồm chuyên luân của các thuốc hay được sử dụng trong thực hành lâm sàng kèm theo các chức năng hỗ trợ tra cứu thông tin như tìm kiếm theo yêu cầu, tra cứu tương tác thuốc, tương hợp – tương kị thuốc tiêm, hỗ trợ kê đơn ...
NEXT >>
ADR REPORT ONLINE
-

Là công cụ cho phép các cán bộ y tế báo cáo phản ứng có hại của thuốc và các vấn đề liên quan đến sử dụng thuốc. Thông tin do các cán bộ y tế cung cấp sẽ vô cùng hữu ích để tiếp tục đánh giá một cách toàn diện hơn về các nguy cơ tiềm ẩn của thuốc khi lưu hành trên thị trường...
NEXT >>
MEDIC ENQUIRY
-

Phần mềm quản lý câu hỏi/trả lời thông tin thuốc được xây dựng với mục đích quản lý, lưu trữ câu hỏi/trả lời một cách khoa học và thuận tiện; đồng thời, giúp việc tìm kiếm thông tin hiệu quả và dễ dàng hơn...
NEXT >>
Articles Search
-
ANSM - Khuyến cáo thuốc có chứa mitomycin C liên quan đến tăng áp lực động mạch phổi và bệnh nghẽn tĩnh mạch phổi
07/06/2017 00:00:00:ANSM thông báo các trường hợp tăng áp lực động mạch phổi và nghẽn tĩnh mạch phổi, bao gồm cả các trường hợp gây tử vong đã được báo cáo ở những bệnh nhân được điều trị với mitomycin C. ...
Next >> -

Health Canada: Điểm một số tin đáng chú ý trong bản tin Health Product InfoWatch số 5 tháng 5/2017
07/06/2017 00:00:00:Một số tin đáng chú ý trong bản tin Health Produc InfoWatch số tháng 5/2017 ...
Next >> -

Lớp đào tạo liên tục về Dược lâm sàng tháng 06/2017
06/06/2017 00:00:00:
Trong khuôn khổ Chương trình đào tạo liên tục về Dược lâm sàng của Trường Đại học Dược Hà Nội, Trung tâm DI & ADR Quốc gia đã ...
Next >> -
.jpg)
ANSM: nhắc lại nguyên tắc trong sử dụng kali clorua đường tĩnh mạch
06/06/2017 00:00:00:Ngày 30/5/2017, ANSM thông báo đã ghi nhận các báo cáo sai sót về thuốc liên quan đến việc tiêm đường tĩnh mạch chế phẩm kali clorua (KCl) nồng độ cao trực tiếp không qua pha loãng. Sai sót này có thể ...
Next >> -
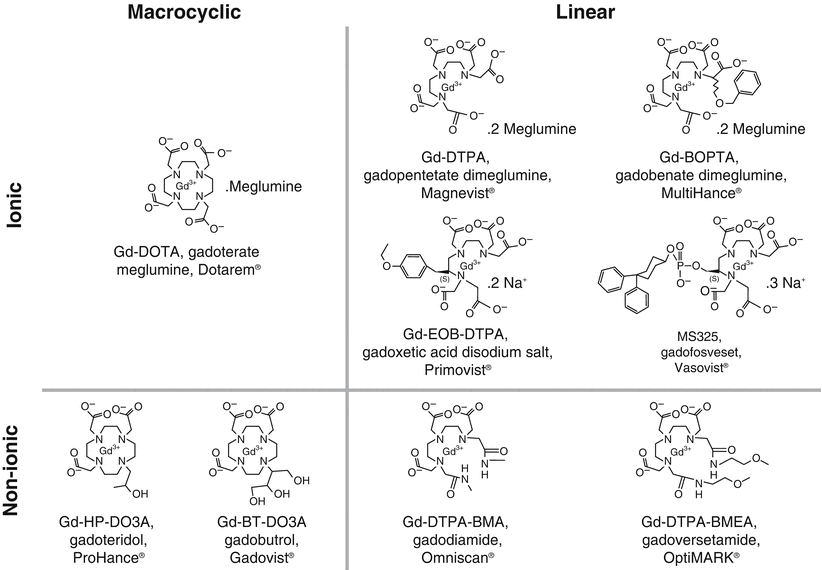
FDA (Mỹ) - Chưa tìm thấy tác hại nào liên quan đến việc tích lũy thuốc cản quang gadolinium trong não
31/05/2017 00:00:00:Qua quá trình thu thập dữ liệu và đánh giá độ an toàn của thuốc, tính đến ngày 22/05/2017, Cơ quan quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) chưa xác định được biến cố có hại nào liên quan đến việc ...
Next >> -
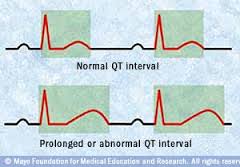
HSA: Khuyến cáo mới trong việc sử dụng domperidon
30/05/2017 00:00:00:Trong bản tin Adverse Drug Reaction News số 1 tập 19 - tháng 5/2017, Cơ quan Khoa học Y tế Singapore (HSA) khuyến cáo nguy cơ tim mạch khi sử dụng domperidon. ...
Next >> -
Bản tin Medicines Safety Update số 2 tháng 4-5/2017: TGA cảnh báo nguy cơ huyết khối động mạch/huyết khối tĩnh mạch khi sử dụng testosteron
26/05/2017 00:00:00:Các cán bộ y tế được cảnh báo lại về liệu pháp điều trị thay thế bằng testosteron nên được kê đơn phù hợp với các chỉ định đã đăng ký và các giới hạn của chương trình Pharmaceutical Benefits Scheme. C ...
Next >> -
EMA: Khuyến cáo thay đổi thông tin kê đơn với các kháng sinh vancomycin
24/05/2017 00:00:00:Ngày 19/5/2017, Cơ quan Quản lý Dược phẩm châu Âu (EMA) đã khuyến cáo thay đổi thông tin kê đơn đối với các kháng sinh vancomycin để đảm bảo sử dụng phù hợp trong điều trị nhiễm khuẩn nặng do vi khuẩn ...
Next >> -

EMA: Hướng dẫn mới về thuốc sinh học tương tự dành cho cán bộ y tế
22/05/2017 00:00:00:Ngày 05/5/2017, Cơ quan Quản lý Dược phẩm châu Âu (EMA) và Ủy ban châu Âu (EC) đã công bố hướng dẫn thông tin dành cho cán bộ y tế về các thuốc sinh học tương tự (biosimilar). Thuốc sinh học tương tự ...
Next >> -

ANSM: Dữ liệu sử dụng và an toàn đối với methylphenidat
18/05/2017 00:00:00:ANSM công bố một báo cáo mới trên cơ sở dữ liệu về tình hình sử dụng tại Pháp và thông tin an toàn với methylphenidat (các biệt dược Ritalin, Ritalin LP, Concerta LP, Quasym LP, Medikinet). Báo cáo nà ...
Next >> -

ANSM: Thông tin về dụng cụ nội tử cung Mirena
17/05/2017 00:00:00:ANSM đã nhận thấy một sự gia tăng báo cáo các phản ứng có hại có thể liên quan đến Mirena (chế phẩm giải phóng levonorgestrel đặt nội tử cung) trong những ngày gần đây. ...
Next >> -

Xuất bản Bản tin Cảnh giác Dược số 1/2017 - bản trực tuyến
15/05/2017 00:00:00:Từ năm 2012 đến nay, để tăng cường hiệu quả hoạt động của hệ thống Thông tin thuốc và Cảnh giác dược, Trung tâm DI &ADR Quốc gia thực hiện việc xuất bản Bản tin Cảnh giác dược. ...
Next >> -
PRAC: Kết luận rà soát về các thuốc chứa yếu tố VIII
15/05/2017 00:00:00:Theo kết quả cuộc họp ngày 02-05/5/2017, PRAC đã hoàn thành rà soát về các thuốc chứa yếu tố VIII với mục đích đánh giá nguy cơ hình thành chất ức chế ở bệnh nhân haemophilia A chưa được điều trị với ...
Next >> -
ANSM điểm lại các bước nghiên cứu đang được thực hiện với docetaxel
13/05/2017 00:00:00:Ngày 02/05/2017, ANSM điểm lại các bước nghiên cứu đang được thực hiện với docetaxel. Các kết quả điều tra của ANSM khẳng định chất lượng đảm bảo của toàn bộ các chế phẩm có chứa docetaxel hiện được l ...
Next >> -
.jpg)
Thuốc thành phẩm chứa phối hợp domperidon và ranitidin chưa có số đăng ký: hồ sơ đăng ký thuốc phải nộp kèm hồ sơ lâm sàng chứng minh tính an toàn, hiệu quả của thuốc.
05/05/2017 00:00:00:Ngày 7 tháng 4 năm 2017, Cục Quản lý Dược (Bộ Y tế) có công văn số 4533/QLD-ĐK gửi các công ty đăng ký, sản xuất thuốc lưu hành tại Việt Nam về việc đăng ký, nhập khẩu đơn hàng thuốc chứa phối hợp dom ...
Next >>
