Tìm kiếm bài viết
-

NSAIDs và nguy cơ sảy thai tự phát (spontaneous abortion)
21/07/2017 12:00:00 SA:Hội đồng Phản ứng có hại của thuốc (Medicines Adverse Reactions Committee - MARC) thuộc MEDSAFE đã công bố biên bản của cuộc họp Hội đồng định kỳ vào ngày 11/07/2017. Trong cuộc họp này, Hội đồng đã t ...
Xem tiếp >> -

Nguy cơ xuất huyết khi sử dụng đồng thời các statin và dabigatran
21/07/2017 12:00:00 SA:Hội đồng Phản ứng có hại của thuốc (Medicines Adverse Reactions Committee - MARC) thuộc MEDSAFE đã công bố biên bản của cuộc họp Hội đồng định kỳ vào ngày 11/07/2017. Trong cuộc họp này, Hội đồng đã t ...
Xem tiếp >> -
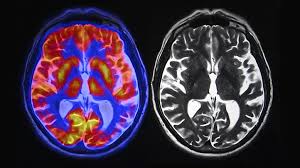
Lắng đọng các thuốc cản quang có chứa gadolinium trong não
21/07/2017 12:00:00 SA:Hội đồng Phản ứng có hại của thuốc (Medicines Adverse Reactions Committee - MARC) thuộc MEDSAFE đã công bố biên bản của cuộc họp Hội đồng định kỳ vào ngày 11/07/2017. Trong cuộc họp này, Hội đồng đã t ...
Xem tiếp >> -

Giới thiệu Bản tin Thông tin Thuốc số 1 – 2017 - Đơn vị Thông tin Thuốc – Bệnh viện Bạch Mai
19/07/2017 12:00:00 SA:Tháng 6/2017, Đơn vị Thông tin Thuốc – Bệnh viện Bạch Mai xuất bản Bản tin Thông tin Thuốc số 1 – 2017. Sản phẩm chuyên môn này là kết quả phối hợp làm việc giữa khoa Dược – Bệnh viện Bạch Mai và Trun ...
Xem tiếp >> -
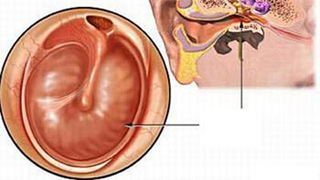
Độ an toàn của một số thuốc nhỏ tai có chứa kháng sinh trên trẻ em có đặt ống thông nhĩ
19/07/2017 12:00:00 SA:Hội đồng Phản ứng có hại của thuốc (Medicines Adverse Reactions Committee - MARC) thuộc MEDSAFE đã công bố biên bản của cuộc họp Hội đồng định kỳ vào ngày 11/07/2017. Trong cuộc họp này, Hội đồng đã t ...
Xem tiếp >> -

Giới thiệu Bản tin Thông tin Thuốc số 1 – 2017 - Đơn vị Thông tin Thuốc – Bệnh viện Bạch Mai
19/07/2017 12:00:00 SA:Tháng 6/2017, Đơn vị Thông tin Thuốc – Bệnh viện Bạch Mai xuất bản Bản tin Thông tin Thuốc số 1 – 2017. Sản phẩm chuyên môn này là kết quả phối hợp làm việc giữa khoa Dược – Bệnh viện Bạch Mai và Trun ...
Xem tiếp >> -

ANSM: cập nhật thông tin về sử dụng các thuốc chứa valproat
18/07/2017 12:00:00 SA:Ngày 06/07/2017, ANSM cảnh báo chống chỉ định dùng các thuốc có chứa valproat điều trị các bệnh tâm thần trên phụ nữ có thai và phụ nữ trong độ tuổi sinh đẻ không có biện pháp tránh thai hiệu quả. ...
Xem tiếp >> -
.jpg)
ANSM: thuốc có chứa codein, dextromethorphan, ethylmorphin và noscapin vào danh mục các thuốc phải kê đơn tại Pháp
17/07/2017 12:00:00 SA:Ngày 12 tháng 7 năm 2017, bộ trưởng Bộ Y tế và Bảo trợ xã hội Pháp đã ký quyết định về việc đưa các thuốc có chứa codein, dextromethorphan, ethylmorphin và noscapin vào danh mục các thuốc phải kê đơn. ...
Xem tiếp >> -
ANSM: Sử dụng thuốc và các chế phẩm y tế trong mùa hè
17/07/2017 12:00:00 SA:Ngoài những người mắc bệnh mạn tính, trẻ sơ sinh và người cao tuổi đều dễ mắc các bệnh trong giai đoạn nắng nóng. Đối tượng có nguy cơ cao là người có các bệnh mắc kèm (đặc biệt bệnh về tim mạch, thận ...
Xem tiếp >> -
ANSM: thông báo gỡ bỏ khuyến cáo tránh sử dụng docetaxel trong ung thư vú và mở rộng phạm vi thực hành
16/07/2017 12:00:00 SA: ...
Xem tiếp >> -
ANSM: thông báo rút khỏi thị trường kem bôi và viên đặt hậu môn Proctolog®
15/07/2017 12:00:00 SA: ...
Xem tiếp >> -

ANSM: cập nhật nguy cơ tổn tổn thương gan nặng khi sử dụng ketamin kéo dài liều cao
14/07/2017 12:00:00 SA:Ngày 04/07/2017, ANSM cập nhật nguy cơ tổn thương gan nặng khi sử dụng ketamin kéo dài liều cao ...
Xem tiếp >> -
.jpg)
TGA: cập nhật thông tin an toàn khi sử dụng tramadol trong thời kỳ cho con bú
13/07/2017 12:00:00 SA: ...
Xem tiếp >> -
EMA: hạn chế sử dụng thuốc đa xơ cứng Zinbryta
12/07/2017 12:00:00 SA:Ngày 07/7/2017, Cơ quan Dược phẩm Châu Âu (EMA) thông báo hạn chế tạm thời việc sử dụng thuốc điều trị đa xơ cứng Zinbryta (daclizumab) trên bệnh nhân đa xơ cứng tái phát hoạt động mạnh không đáp ứng ...
Xem tiếp >> -
Hội thảo Tổng kết dự án giai đoạn 2012-2016 trong khuôn khổ dự án “Hỗ trợ hệ thống y tế”
11/07/2017 12:00:00 SA:Nhằm tổng kết các kết quả hoạt động đã triển khai giai đoạn 2012-2016, Ban quản lý dự án “Hỗ trợ hệ thống y tế” tổ chức Hội thảo Tổng kết dự án giai đoạn 2012-2016 ngày 30/6-01/7/2017 tại Phú Yên. ...
Xem tiếp >>

