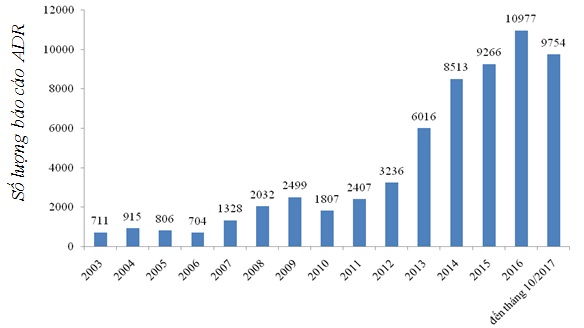
Với mục tiêu cập nhật về tình hình báo cáo phản ứng có hại của thuốc (ADR) và thúc đẩy triển khai hoạt động này tại các cơ sở khám chữa bệnh, hướng tới sử dụng thuốc hợp lý, an toàn, Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc (Trung tâm DI&ADR Quốc gia) đã tiến hành xử lý, phân tích các thông tin từ báo cáo phản ứng có hại của thuốc nhận được từ cán bộ y tế, các cơ sở khám bệnh, chữa bệnh và các đơn vị sản xuất, kinh doanh dược phẩm trên phạm vi toàn quốc.
Việc tổng kết công tác báo cáo ADR được thực hiện hàng năm và gửi tới các Cục, Vụ chức năng của Bộ Y tế, các chương trình mục tiêu quốc gia về y tế, các Sở Y tế, các bệnh viện, viện có giường bệnh trực thuộc Bộ Y tế và các đơn vị đã tham gia gửi báo cáo ADR trong năm 2017. Trung tâm DI&ADR Quốc gia xin trân trọng gửi đến quý đơn vị báo cáo tổng kết hoạt động báo cáo ADR năm 2017 (tính đến ngày 31/10/2017).
Nội dung chi tiết xem tại đây.
Bên cạnh đó, để phục vụ công tác kiểm tra, đánh giá chất lượng bệnh viện, từ năm 2018, Trung tâm DI&ADR Quốc gia sẽ tổng kết công tác báo cáo ADR từ tháng 11 năm trước đến hết tháng 10 của năm kế tiếp.
Trong quá trình xử lý báo cáo ADR, Trung tâm nhận thấy có một số báo cáo ADR gửi từ các đơn vị và thư cảm ơn, phản hồi từ Trung tâm bị thất lạc qua đường bưu điện. Để đảm bảo việc trao đổi thông tin được đầy đủ, kịp thời, Trung tâm xin đề nghị các đơn vị tăng cường triển khai báo cáo bằng các hình thức khác (báo cáo trực tuyến, gửi thư điện tử hoặc fax) bên cạnh hình thức gửi báo cáo qua đường bưu điện về trung tâm. Cũng từ năm 2018, Trung tâm dự kiến sẽ gửi thư cảm ơn, phản hồi và các thông tin khác về ADR cho các đơn vị qua đường thư điện tử. Trong trường hợp có nhu cầu, đề nghị các đơn vị gửi công văn đề xuất 01 cán bộ đầu mối và 01 lãnh đạo khoa/phòng phụ trách công tác Cảnh giác Dược để nhận các thông tin nêu trên (công văn cần ghi rõ họ tên, chức vụ, đơn vị, số điện thoại và địa chỉ email của các cá nhân được đề xuất).
Trung tâm trân trọng cám ơn sự đóng góp của Quý đơn vị trong năm 2017 và mong tiếp tục nhận được sự hợp tác để triển khai tốt hoạt động báo cáo phản ứng có hại của thuốc theo qui định hiện hành của Bộ Y tế.
Người tổng hợp: DS. Trần Ngân Hà