Tổng quan độ an toàn đối với nguy cơ phản ứng dị ứng nghiêm trọng liên quan đến Chlorhexidin
Lưu ý chính:
- Chlorhexidin được biết đến là hiếm gây các trường hợp mẫn cảm, bao gồm các phản ứng dị ứng toàn thân và sốc phản vệ
- Các chế phẩm chlorhexidin không nên sử dụng cho bệnh nhân có tiền sử hoặc nghi ngờ dị ứng chlorhexidin. Nhãn thuốc và hướng dẫn sử dụng cần được kiểm tra để xác định chế phẩm có chlorhexidin không trước khi sử dụng cho bệnh nhân có dị ứng thuốc
- Mặc dù tỷ lệ mẫn cảm chlorhexidin là hiếm gặp, song cán bộ y tế nên cảnh giác với nguy cơ phản ứng dị ứng nghiêm trọng có thể xảy ra, bao gồm sốc phản vệ
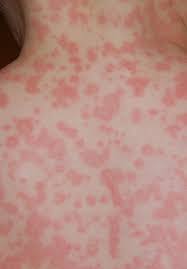
Chlohexidine là chất sát trùng phổ rộng diệt được các loại vi khuẩn Gram (+) và Gram (-) trên da, thuốc được sử dụng rộng rãi để giảm nguy cơ nhiễm trùng do vi khuẩn. Chlohexidine có mặt trong nhiều loại chế phẩm sát trùng bôi trên da hoặc niêm mạc miệng trong các dạng thuốc như kem bôi, chất tẩy rửa, nước súc miệng, thủ thuật nha khoa, viên ngậm, thuốc gây tê tại chỗ và băng gạc diệt khuẩn. Một số catheter đặt trong cơ thể như các catheter niệu và các catheter tĩnh mạch trung tâm cũng có thể được tráng hoặc ngâm tẩm chlorhexidine để ngăn ngừa nhiễm khuẩn liên quan đến catheter.
(Ảnh: nguồn internet)
Các hoạt động quản lý trên thế giới
(a) US FDA
Tháng 2/2017, US FDA đưa ra thông tin an toàn liên quan đến các phản ứng dị ứng nghiêm trọng với các chế phẩm sát trùng trên da có chứa chlorhexidine gluconat. Mặc dù là hiếm gặp, US FDA chia sẻ rằng số lượng báo cáo biến cố bất lợi của các phản ứng dị ứng nghiêm trọng của các chế phẩm này tăng qua 5 thập kỷ vừa qua và khuyến cáo nhãn của các chế phẩm bán không cần kê đơn của các chế phẩm có chứa chlorhexidin gluconat cần được cập nhật với cảnh báo và khả năng gây phản ứng dị ứng nghiêm trọng. Cảnh báo này hiện tại có trên các nhãn nước súc miệng có chlorhexidin gluconat cần kê đơn để điều trị viêm nướu và các loại bột uống kê đơn điều trị bệnh nha chu. US FDA đã xác định 43 trường hợp nghiêm trọng trên toàn cầu về phản ứng phản vệ khi sử dụng chế phẩm chứa chlohexidin gluconat dùng tại chỗ. Các trường hợp này được báo cáo tới Hệ thống báo cáo biến cố bất lợi của FDA từ tháng 1/1969 đến tháng 6/2015, trong đó có 24 (56%) trường hợp được báo cáo sau 2010. Các trường hợp nghiêm trọng được báo cáo và chúng bao gồm tình trạng đe dọa tính mạng (26 trường hợp), nhập viện (12 trường hợp) và tử vong do sốc phản vệ (2 trường hợp). Tất cả các trường hợp được báo cáo liên quan chặt chẽ về thời gian sử dựng chế phẩm chứa chlorhexidin gluconat, với 7 trường hợp được báo cáo phản ứng dị ứng tái phát. Thêm vào đó, có 9 trường hợp phản ứng phản vệ liên quan đến chlorhexidin được xác định từ y văn và cơ sở dữ liệu giám sát biến cố bất lợi Quốc gia (NEISS-CADES).
(b) Cơ quan Quản lý y tế Canada
Health Canada đưa ra thông tin an toàn vào tháng 5/2016 về nguy cơ các phản ứng quá mẫn nghiêm trọng với sử dụng các chế phẩm sát trùng không kê đơn tại chỗ có chlorhexidin. Đánh giá về độ an tonaf này được thực hiện trên 53 báo cáo trong nước về các phản ứng dị ứng nghiêm trọng với sử dụng chế phẩm tại chỗ không kê đơn chứa chlorhexxidin, bao gồm 03 phản ứng phản vệ, cũng như các trường hợp đã được công bố trong y văn. Health Canada kết luận rằng mặc dù không phổ biến, một vài tình trạng có thể tăng nguy cơ phản vệ, ví dụ như sử dụng chlorhexidin trong miệng, trên các vết thương hở, hoặc ngay trước hoặc trong phẫu thuật. Do vậy, Health Canada khuyến cáo rằng cập nhật thông tin sản phẩm của các chế phẩm chứa chlorhexidin không kê đơn với những phát hiện mới này.
(c) Cơ quan Quản lý khác
Các cơ quan Quản lý dược phẩm của Úc, Anh, New Zealand cũng có cảnh báo an toàn tương tự từ năm 2009 đến 2013. Các cơ quan này thông báo đến cán bộ y tế về nguy cơ phản ứng quá mẫn nghiêm trọng khi sử dụng chế phẩm chứa chlorhexidin, bao gồm các chế phẩm gel gây tê tại chỗ và các catheter tĩnh mạch trung tâm được ngâm tẩm chlorhexidin. Các cơ quan quản lý cũng nhắc lại với cán bộ y tế rằng chlorhexidin được biết tới là dẫn đến quá mẫn và rằng các chế phẩm thay tế nên được sử dụng nêu CBYT nghi ngờ bệnh nhân dị ứng với chlorhexidin. Nhãn thuốc và hướng dẫn sử dụng nên được kiểm tra các chế phẩm hoặc dụng cụ có chứa chlorhexidin hay không trước khi sử dụng cho các bệnh nhân có tiền sử dị ứng với chất này
Các kết quả đánh giá của HSA
Đánh giá hiện tại của HSA trên các báo cáo biến cố bất lợi kết luận rằng tổng số báo cáo AE mà HAS nhận được liên quan đến quá mẫn chlorhexidin tăng không có ý nghĩa thông kê qua các năm. Phần lớn các báo cáo được mô tả là báo cáo AE không nghiêm trọng như ngứa hoặc nổi mẩn. Mười lăm báo cáo phản ứng phản vệ liên quan đến chlorhexidin được xác định trong khoảng 36 năm (từ 1981 đến 2017). Không có xu hướng gia tăng phản ứng dị ứng nghiêm trọng với chế phẩm chứa chlohexidin qua nhiều năm. Đánh giá của HAS không xác định được bất cứ tín hiệu an toàn nào trong nước liên quan đến phản ứng dị ứng nghiêm trọng khi sử dụng chlorhexidin tại thời điểm này. Có thể hiểu rằng, có thể có một số trường hợp chlorhexidin dẫn đến các phản ứng dị ứng nghiêm trọng có thể không được báo cáo do mối quan hệ nhân quả với tác nhân gây bệnh có thể không rõ ràng. Tuy nhiên, HSA sẽ tiếp tục theo dõi mối quan ngại về độ an toàn này và sẽ có động thái thích hợp và kịp thời nếu cần thêm các biện pháp để giảm thiểu rủi ro.
Khuyến cáo của HSA
Chlorhexidin có thể dẫn tới phản ứng quá mẫn, bao gồm các phản ứng dị ứng toàn thân và sốc phản vệ. Mặc dù tỷ lệ quá mẫn với chlorhexidin là hiếm gặp, các cán bộ y tế được khuyến cáo cảnh giác với nguy cơ các phản ứng quá mẫn nghiêm trọng, bao gồm sốc phản vệ với các chế phẩm chứa chlorhexidin. Nhãn thuốc và hướng dẫn sử dụng cần được kiểm tra xem chế phẩm có chứa chlorhexidin hay không trước khi sử dụng trên bệnh nhân nghi ngờ hoặc xác định có tiền sử dị ứng với chlorhexidin. Các cán bộ y tế được khuyến cáo thông tin cho bệnh nhân dừng sử dụng chế phẩm và tìm sự chăm sóc y tế ngay lập tức nếu họ gặp các triệu chứng của phản ứng dị ứng nghiêm trọng như thở khò khe, sưng mặt hoặc phát ban nghiêm trọng.
Nguồn: http://www.hsa.gov.sg/content/dam/HSA/HPRG/Safety_Alerts_Product_Recalls_Enforcement/
Adverse_Drug_Reaction_News/2017/ADR_News_Sep2017_Vol19_No2.pdf
Điểm tin: Nguyễn Thị Tuyến